С.Д. Цибуля, канд. техн. наук
Н.П. Буяльська, канд. техн. наук
Чернігівський державний технологічний університет, м. Чернігів, Україна
В.Г. Старчак, д-р техн. наук
Г.М. Мачульський, канд. сільгосп. наук
Чернігівський національний педагогічний університет імені Т.Г. Шевченка, м. Чернігів, Україна
КОМПЛЕКСНЕ ЗАБЕЗПЕЧЕННЯ ЯКОСТІ ЗАХИСТУ ВІД КОРОЗІЇ
На основі комплексного системного кореляційного аналізу «Електронна структура, термодинамічні параметри Ін – захисні, адсорбційні властивості» здійснено вибір оптимального синергіста в складі синергічної захисної композиції (СЗК) на вторинній сировині. При виборі оптимального інгібітора враховано: здатність складових до N-, О-, S-, С-протонування, депротонування, утворення карбаніонів; електронну структуру та термодинамічні параметри, в залежності від форм дії – молекулярної, катіонної, аніонної. Розроблена СЗК забезпечує комплексний захист сталі від загальної корозії, наводнювання та від основної причини техногенних аварій – корозійної втоми, корозійного розтріскування та водневої деградації, за рахунок модифікації поверхні металовиробів наномасштабними металохелатними плівками.
Вступ
Відомо, що корозійні процеси, особливо в кислих, лужних, Н2s-вмісних середовищах, супроводжуються наводнюванням, яке часто більш небезпечне, ніж, власне, корозія. Інтенсивність його залежить від багатьох факторів: структури сталі (зменшення поглинання водню в ряду – аустеніт, перліт, мартенсит, троостит; дрібнозерниста сталь поглинає водню більше ніж крупнозерниста). З маловуглецевої сталі водень десорбується (на 90%) протягом 7 діб (за одну добу – 50%). Десорбцію уповільнюють Ті, V, Cr, Zr, Nb. З підвищенням в сталі вмісту вуглецю, холодної деформації, мартенситної складової підсилюється воднева крихкість. У ланках, що збагачені воднем, формується пористість, тріщини. В деформованому фериті розчинність водню в 2…3 рази вище, ніж у недеформованому. Водень знижує температуру мартенситного перетворення, гальмує рухомість вакансій [1-4].
Водень, що потрапив до металу, змінює його адсорбційні властивості. Специфічна адсорбція Ін може частково виключити розряд Н+ та, таким чином, сприяти переносу електронів на ліганд (з утворенням π-дативних зв'язків). Протонування передує стадії переносу заряду. Протонована молекула Ін відновлюється легше, ніж непротонована. За правилом електронегативності (ЕН) Шиката та Тачі: із збільшенням ЕН замісників у молекулі та числа подвійних зв'язків спостерігається полегшення відновлення молекул Ін. Певну роль в електронному переносі грають полярні (індукційні), мезомерні та стеричні ефекти замісників. Металохелатування відбувається за умови: СL (СНхL) більше СМ (СL, СНхL, СМ – концентрації вільних, зв'язаних лігандів, катіонів металу) [5; 6].
Мета роботи – провести вибір ефективного, поліфукціонального Ін на основі комплексного системного кореляційного аналізу.
Методи дослідження
Дослідження проведено за комплексною системою оцінки ефективності захисту сталі 20, 45 та ін. в корозійно-наводнювальних середовищах із застосуванням гравіволюмометрії, електрохімічних методів (потенціостат П5827М), фізико-механічних випробувань (на малоциклову втому – ІП-2, корозійне розтріскування) [7-11]. За mndo-РМ3 здійснено розрахунок термодинамічних характеристик та електронної структури і визначено потенціальні найбільш активні адсорбційні центри (АЦ).
Результати експерименту та їх обговорення
Експериментальні дані представлено в табл. 1-3 та на рис. 1, 2.
Таблиця 1
Термодинамічні параметри та електронна структура Ін 1
|
Характе-ристики |
Ін |
|||
|
Mol |
Kat 1 |
Kat 2 |
An |
|
|
ΔHf, кДж/моль |
102,41 |
683,59 |
895,32 |
38,67 |
|
І, еВ |
8,59 |
12,75 |
11,61 |
4,20 |
|
-Еп, еВ |
3095,09 |
3104,40 |
3102,15 |
3080,42 |
|
-Еел, еВ |
22945,55 |
23435,17 |
23353,71 |
22954,85 |
|
μ, D |
2,78 |
- |
- |
- |
|
q, на: |
|
|
|
|
|
N3 |
-.10761 |
.39507 |
-.05922 |
-.10767 |
|
N1 |
.26137 |
.37190 |
.17340 |
.36066 |
|
S |
.09270 |
.21121 |
.10692 |
.07360 |
|
O |
-.31126 |
-.30120 |
-.14116 |
-.75638 |
|
Ph |
-.57015 |
-.58648 |
-.60107 |
-.70859 |
|
|
Kat 1 – протонування по N3, Kat 2 – по О. |
|||
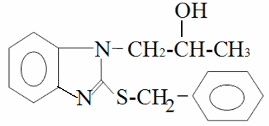
Рис. 1. Хімічна будова Ін 1
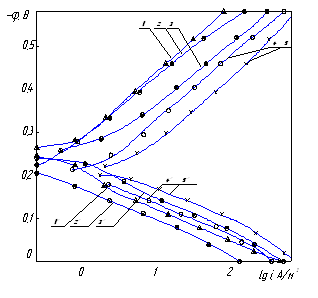
Рис. 2. Поляризаційні катодні (1–5) і анодні (1/–5/) криві на сталі 45 у
2М HCl: 1,1/ – Ін 1; 2,2/ – Iн 2; 3,3/ – К; 4,4/ – КУБ; 5,5/ – без Ін
Максимальну реакційну здатність Ін 1 по утворенню металохелатів підтверджено даними табл.1 та захисними інгібуючими ефектами (рис. 2, табл. 2, 3), що дало змогу розробити синергічну захисну композицію (СЗК) на вторинній сировині (відходи ЧП «Хімволокно» – К, РХП «Азот» – КУБ).
Таблиця 2
Кінетичні та термодинамічні параметри корозії сталі у 2М HCl
|
Ін |
Густина струму, А/м2 |
- φс, В |
ak, В |
aa, В |
Rр, */ мОм·м2 |
|||
|
ic |
ik |
ia |
1 |
2 |
||||
|
– |
1,20 |
79,40 |
7,94 |
0,19 |
0,80 |
0,67 |
17,3 |
8,1 |
|
Ін 1 |
0,13 |
3,16 |
5,00 |
0,25 |
1,00 |
0,71 |
159,5 |
59,3 |
|
*/1 – сталь 20, 2 – сталь 45 |
||||||||
Таблиця 3
Захисні ефекти Ін 1 у 2М HCl
|
Сталь |
γ1 |
γ2 |
γ3 |
γс |
γх |
γ Σ |
z, % |
β,% |
|
20 |
1,6 |
6,5 |
6,1 |
9,2 |
5,0 |
14,2 |
93,0 |
75,3 |
|
45 |
1,7 |
5,5 |
6,2 |
7,3 |
6,1 |
13,4 |
92,5 |
71,8 |
Протонування молекули Ін 1 по піридиновому азоту (N3-атому) приводить до значного підвищення позитивного заряду на N1-, N3-атомах та атомі S, що сприяє утворенню π-дативних зв’язків, з переносом заряду на ліганд (М![]() L), із зв’язуючими молекулярними орбіталями (МО). Цьому сприяє обмеженість утворення π-донорно-акцепторних зв’язків із розрихляючими МО, за рахунок значної величини потенціалу іонізації катіону (1) – 12,75 еВ. Індуктивний ефект алкільного замісника підвищує хемосорбційну властивість ендоатомів N та S. В результаті утворюються щільні екрануючі шари, що заважають перебігу електродних реакцій, у тому числі розряду іонів гідроксонію. Це підтверджується значним інгібуванням наводнювання (β=71,8…75,3%), а також парціальними інгібуючими ефектами γ2> γ3> γ1, (сталь 20), та γ3> γ2> γ1 (сталь 45). Це означає, що Ін 1 діє як активаційно-блокувальний. При протонуванні молекули Ін 1 по екзоатому О, можливість утворення π-дативних зв'язків менша за протонування по N3-атому та вільної молекули Ін: позитивний заряд на N1 знижується майже в 2 рази. Активізація Ін 1 здійснюється також за рахунок його дії як карбаніону при депротонуванні молекули. До того ж криві ЕКК (σ, Е-криві) підтверджують його дію як аніоноактивного Ін (Е(0) зміщується в негативний бік). Спостерігається активізація електронодонорних центрів – на атомі О (електронна густина зростає майже в 2,5 рази), досягає максимального значення електронна густина на нуклеофільному центрі – на Рh. Це сприяє утворенню π-донорно-акцепторних зв'язків. До того ж складний замісник –s–СН2–С6Н5 по атому С2 обумовлює позитивний мезомерний ефект (+М), який збагачує електронну густину в орто- та пара-положеннях Рh-кільця, що підсилює π-донорно-акцепторну взаємодію (L
L), із зв’язуючими молекулярними орбіталями (МО). Цьому сприяє обмеженість утворення π-донорно-акцепторних зв’язків із розрихляючими МО, за рахунок значної величини потенціалу іонізації катіону (1) – 12,75 еВ. Індуктивний ефект алкільного замісника підвищує хемосорбційну властивість ендоатомів N та S. В результаті утворюються щільні екрануючі шари, що заважають перебігу електродних реакцій, у тому числі розряду іонів гідроксонію. Це підтверджується значним інгібуванням наводнювання (β=71,8…75,3%), а також парціальними інгібуючими ефектами γ2> γ3> γ1, (сталь 20), та γ3> γ2> γ1 (сталь 45). Це означає, що Ін 1 діє як активаційно-блокувальний. При протонуванні молекули Ін 1 по екзоатому О, можливість утворення π-дативних зв'язків менша за протонування по N3-атому та вільної молекули Ін: позитивний заряд на N1 знижується майже в 2 рази. Активізація Ін 1 здійснюється також за рахунок його дії як карбаніону при депротонуванні молекули. До того ж криві ЕКК (σ, Е-криві) підтверджують його дію як аніоноактивного Ін (Е(0) зміщується в негативний бік). Спостерігається активізація електронодонорних центрів – на атомі О (електронна густина зростає майже в 2,5 рази), досягає максимального значення електронна густина на нуклеофільному центрі – на Рh. Це сприяє утворенню π-донорно-акцепторних зв'язків. До того ж складний замісник –s–СН2–С6Н5 по атому С2 обумовлює позитивний мезомерний ефект (+М), який збагачує електронну густину в орто- та пара-положеннях Рh-кільця, що підсилює π-донорно-акцепторну взаємодію (L![]() М), якій сприяє низьке значення І (в 2 рази менше за Іmol та в 3 рази за Іkat). Це інтенсифікує утворення π-металохелатів за донорно-акцепторним механізмом. Разом з тим, електроноакцепторний центр (на N1-атомі) має теж високу активність, близьку до протонованої молекули (1).
М), якій сприяє низьке значення І (в 2 рази менше за Іmol та в 3 рази за Іkat). Це інтенсифікує утворення π-металохелатів за донорно-акцепторним механізмом. Разом з тим, електроноакцепторний центр (на N1-атомі) має теж високу активність, близьку до протонованої молекули (1).
За результатами гравіволюмометрії, поляризаційними кривими, даними витривалості сталі в умовах циклічного та статичного навантаження (МЦКВ, МЦВВ, КР) встановлено оптимальні концентрації складових у СЗК: 10г/л К (КУБ)+1 ммоль/л Ін 1. Це відповідає співвідношенню СL (СНхL)=5…7 См. Активною складовою К, КУБ є амідні групи в складі ε-К, його олігомерів, де атоми С, N, О мають sp2-гібридизацію і проявляють негативний індукційний та мезомерний ефекти (σ-константи Гамета σм = 0,28, σп = 0,36, σ![]() = 0,61). Це активізує протонування як по N-, О-, так і С-атомам. СЗК діє як Ін з блокувальною дією γ3> γ2> γ1 >γ4. Ефективність захисту сталі 20 у 2М HCl із СЗК складає (при ε=0,2%): z=97,5 та β=75%. γснN=1,9; ККР (сталь 45, ε=0,4%) дорівнює 120, γсин=1,5…3,5. Наявність стійкої металохелатної захисної плівки підтверджено Оже-, ІЧ-спектрами (Jamp 10S, UR-10) та рентгеноспектральним аналізом (Superprobe 733 Jeol). Характерно, що розроблена СЗК має екологічні переваги: 4 клас небезпеки – малонебезпечні речовини, тоді як такі технічні Ін, як ХОСП-10, уротропін, МСДА, МДА мають 2 клас небезпеки – високонебезпечні речовини.
= 0,61). Це активізує протонування як по N-, О-, так і С-атомам. СЗК діє як Ін з блокувальною дією γ3> γ2> γ1 >γ4. Ефективність захисту сталі 20 у 2М HCl із СЗК складає (при ε=0,2%): z=97,5 та β=75%. γснN=1,9; ККР (сталь 45, ε=0,4%) дорівнює 120, γсин=1,5…3,5. Наявність стійкої металохелатної захисної плівки підтверджено Оже-, ІЧ-спектрами (Jamp 10S, UR-10) та рентгеноспектральним аналізом (Superprobe 733 Jeol). Характерно, що розроблена СЗК має екологічні переваги: 4 клас небезпеки – малонебезпечні речовини, тоді як такі технічні Ін, як ХОСП-10, уротропін, МСДА, МДА мають 2 клас небезпеки – високонебезпечні речовини.
Висновки
Комплексний системний кореляційний аналіз «Електронна структура, термодинамічні параметри Ін – захисні, адсорбційні властивості» дає можливість здійснити вибір оптимального синергіста в складі СЗК на вторинній сировині, з активізацією його дії в молекулярній, катіонній, аніонній формах Ін, що забезпечує високу якість захисту сталі від корозії, наводнювання, малоциклової втоми, корозійного розтріскування.
Список використаних джерел
1. Сучасне матеріалознавство ХХІ сторіччя / відп. редактор акад. І.К. Походня. – К.: Наук. думка, 1998. – 658с.
2. Механіка руйнуваня матеріалів і міцність конструкцій / під ред. акад. В.В. Панасюка. – Львів: Каменяр, 1999. – Т.1 – 352 с., Т.2 – 346 с., Т.3 – 286с.
3. Шаповалов В.И. Флокены и контроль водорода в стали / Шаповалов В.И., Трофименко В.В. – М.: Металлургия, 1987. – 160с.
4. Похмурський В.І. Корозійно-механічне руйнування зварних конструкцій / Похмурський В.І., Мелехов Р.К., Круцан Г.М. – Київ: Наук. думка, 1995. – 262 с.
5. Organic electrochemistry. An Introduction and Guide / edited by M.Baizer. Corporate Research Depart. St. Louis Missouri. – New York: Marcel Dekker, 1973. – 732p.
6. Помогайло А.Д., Уфлянд Н.Е. Макромолекулярные металлохелаты / Помогайло А.Д., Уфлянд Н.Е. – М.: Химия, 1991. – 304с.
7. Старчак В.Г. Комплексная система контроля и оценки эффективности защиты сталей от коррозионно-механических разрушений в наводороживающих средах / Старчак В.Г. – Чернигов: ВСНТО, 1983. – 69с.
8. Старчак В.Г. Повышение стойкости стали в электрохимических процессах: автореф. дис. … докт. техн. наук: 05.17.14, 05.17.03 / Старчак В.Г.; КПИ. – Киев, 1988. – 37 с.
9. Наукові основи підвищення екологічної безпеки металоконструкцій модифікацією їх поверхні в протикорозійному захисті / В.Г. Старчак, Н.П. Буяльська, С.Д. Цибуля та ін. // Фіз.-хім. механіка матеріалів. Спец. випуск. – 2004. – №4. – Т. 2. – С. 853-859.
10. Старчак В.Г. Роль гетероатомов в образовании металлохелатных наноструктур при поверхностной модификации материалов / Старчак В.Г., Алексеенко С.А., Буяльская Н.П. // Наноструктурное материаловедение. – 2008. – ІV-ХІІ. – С.70-84.
11. Старчак В.Г. Екологічна безпека конструкційних матеріалів / Старчак В.Г., Бондар О.І. – К.: ДЕІ, 2008. – 40с.




